ロドプシンの吸収波長は、その蛋白質機能を語る
レチナール蛋白質である微生物型ロドプシンは発色団としてレチナール・シッフ塩基を持ちます。石北研究室では
- プロトンポンプ:bacteriorhodopsin (BR), Rubrobacter xylanophilus rhodopsin(RxR)
- センサー:Anabaena sensory Rhodopsin (ASR), Sensory rhodopsin II (SRII)
- カチオンチャネル:channelrhodopsin-1・channelrhodopsin-2キメラ蛋白質(C1C2)
- カチオンポンプ:sodium pump rhodopsin from Krokinobacter eikastus(KR2)
- クロライドポンプ:halorhodopsin (HR), eubacterial chloride pumping rhodopsin (ClR)
らの異なる機能を持つ13種の微生物型ロドプシン蛋白質結晶構造をもとに吸収波長計算を行いました。
わかったことの一つは、DFT計算によるHOMO-LUMOエネルギー差とTDDFT計算励起エネルギー計算を行いました。特に、DFT計算によるHOMO-LUMOエネルギー差では吸収波長実験値と非常に高い相関を得ました。DFT計算によるHOMO-LUMOエネルギー差の報がTDDFTによる励起エネルギー計算よりも高い相関を示すことは、他のレチナール蛋白質においても経験的にわかっており、紛れもない事実です(論文)。
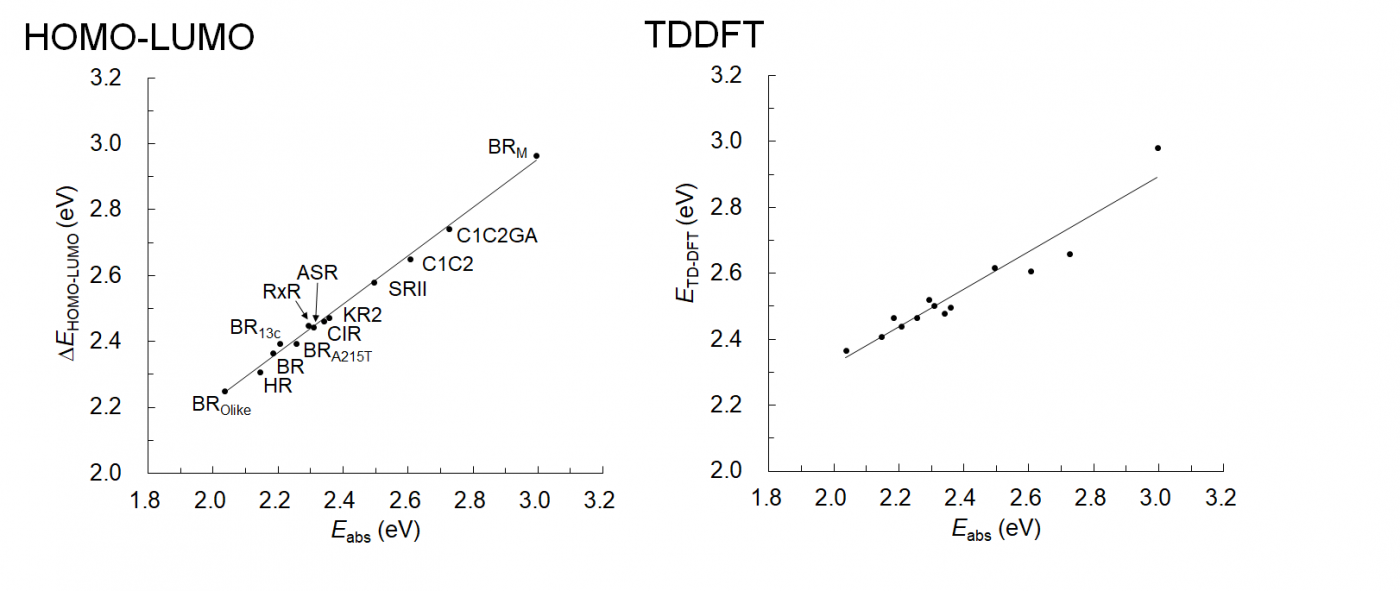
わかったことの二つ目として、微生物型ロドプシン蛋白質の吸収波長は、蛋白質の静電総合作用でほぼ決まっており、しかもカウンターイオンといわれるレチナール・シッフ塩基に近接するたかだか3つの解離性・極性残基との相互作用(つまるところ、アミノ酸残基の電荷と、レチナール。シッフ塩基までの距離)が支配的であるという事実です。これが今回の石北研究室の成果として初めて明らかになりました。
非常に面白いことに、蛋白質環境によるレチナール・シッフ塩基への相互作用は以下の順番で強くなっていきます:
- センサー蛋白質
- プロトンポンプ
- クロライドポンプ
- カチオンチャネル・カチオンポンプ
実際、センサー蛋白質ASRではカウンターイオンでの解離性残基は一つしか存在しませんが、カチオンチャネル・カチオンポンプでは二つの解離性残基と一つの極性残基が存在し、明らかに静電場環境が異なります。
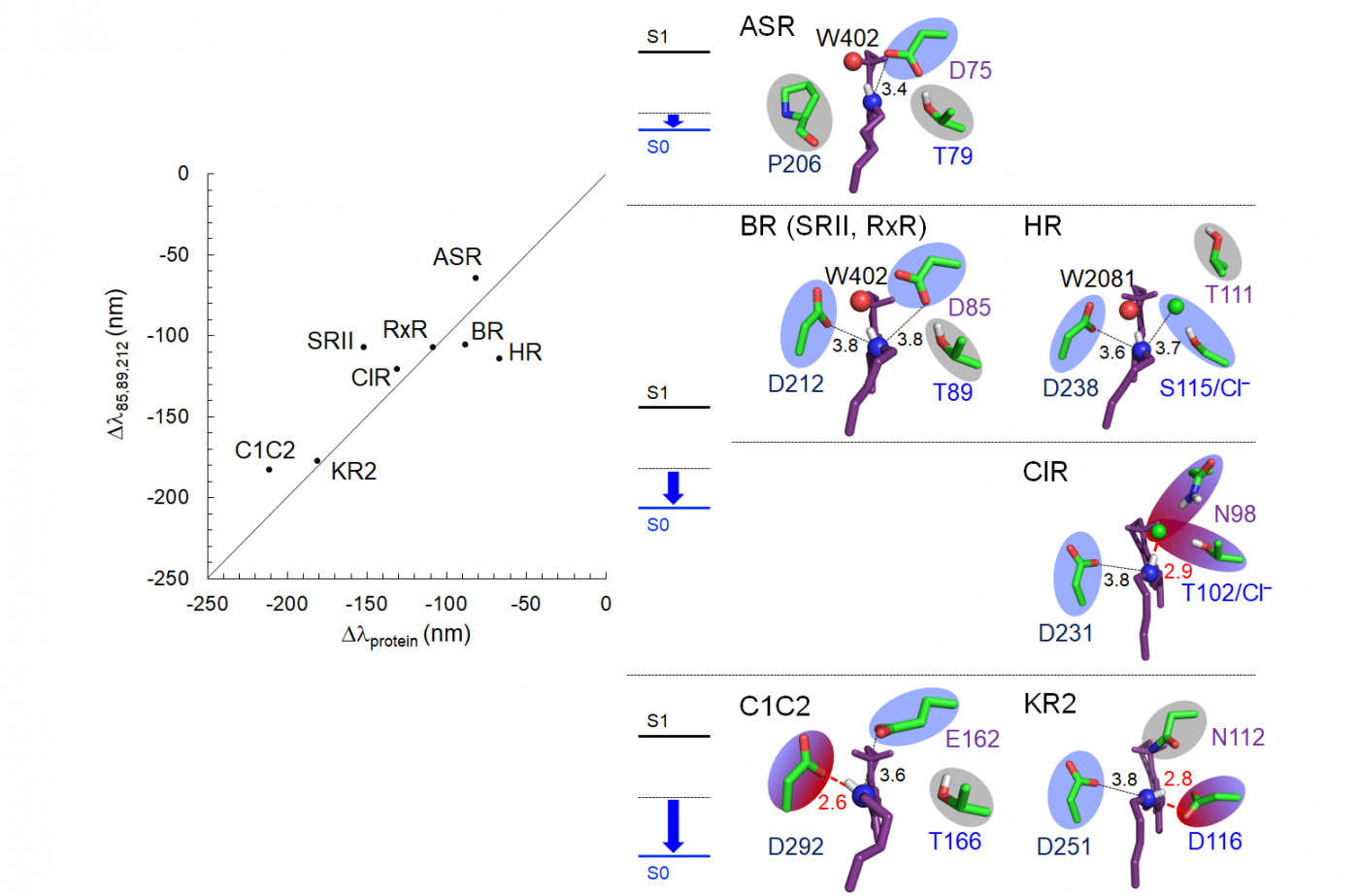
この研究でわかった重要な点の3番目は、テクニカルなことです。レチナール蛋白質の場合、オリジナルの結晶構造座標の利用で吸収波長は正しく求められる、ということです。実際、結晶構造においてレチナール・シッフ塩基近傍のアミノ酸のゆらぎは特に小さいことが結晶構造解析結果から見て取れます。それは少し考えれば当然のことで、レチナール・シッフ塩基は膜貫通ヘリックスに囲まれた領域に存在し、かつ膜の真ん中近くにあるからです。そのような環境に、カウンターイオンという解離性、あるいは極性残基が存在すれば、その影響が支配的であるのは容易に理解できると思います。よく揺らぐ部位は膜貫通部位から外の蛋白質表面残基であり、
- 長距離のため静電相互作用が弱い
- バルク表面に露出しているため部分的に静電相互作用が遮蔽されること
- レチナール・シッフ塩基からみれば、遠方での揺らぎは相対的により小さく見えること
等で吸収波長ピーク値にはほとんど影響は出ません。

事実、分子動力学計算も試しに行い複数のコンフォメーションから吸収波長計算も行い比較しましたが、結局得られる相関は、アンサンブルとしてばらつきが出る分、悪くなります。分子動力学計算は伝家の宝刀でも何でもなく、うまくいっている分子動力学計算ほど安定な構造の近傍で平衡状態を再現するだけであり、それ以上のものは出てきません。かえって、満足できるパラメーターを用いない限りおかしな構造を作り出してしまう可能性すらあります。また、オリジナルの結晶構造で電子密度が見られていないポジションに原子があることの妥当性うぃ示すには、相当の検証の努力が必要ですが、その検証の努力なしで数値のみはじき出して「実験値と計算値は一致した」という態度では、サイエンスでも何でもありません。いくつかの既存の分子動力学計算を併用した研究では、誤ったアミノ酸解離状態による結果で吸収波長を計算しており、構造もおかしくなっています。そのようなartifactな構造による計算結果が正しいとは到底主張できないでしょう。
以上の3つの主な結果は、世界で初めて石北研究室が明らかにした事実であり、以下の論文に記載されています。引用してご活用ください。
Masaki Tsujimura and Hiroshi Ishikita*
J. Phys. Chem. B (2020) doi: 10.1021/acs.jpcb.0c08910
“Insights into the protein functions and absorption wavelengths of microbial rhodopsins”
Journal Pubmed


