低障壁水素結合は通常の水素結合に比べて短めな傾向はありますが、その判定には水素結合ポテンシャルエナジー曲線の解析により左右対称の形状になることが必要です(記事参照)。
さて、一般的な水素結合のドナー・アクセプター原子間距離を強引に(エネルギーを費やして)近づけていった場合、低障壁水素結合となるのでしょうか。これに関して、とてもわかりやすい例があります。
石北研究室により初めて低障壁水素結合であることが示されたものに、photosystem II (PSII)の酸化還元活性を持つD1-Tyr161 (TyrZ)とD1-His190間の水素結合があります。
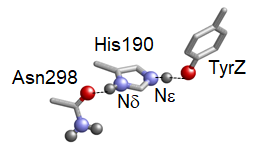
図 PSII蛋白質環境中におけるTyrZ…D1-His190間の低障壁水素結合
この低障壁水素結合を例にとって、説明します。このTyrZ…D1-His190の低障壁水素結合はO…N距離が2.47 Åと非常に短いです。が、この長さで最も安定なのです。試しにドナー・アクセプター原子間の距離を伸ばしていこうとすると、以下の図でわかるようにエネルギーを要します(図、赤矢印)。一方で、距離が伸びても水素結合ポテンシャルエナジー曲線は左右対称の形状を維持しています。
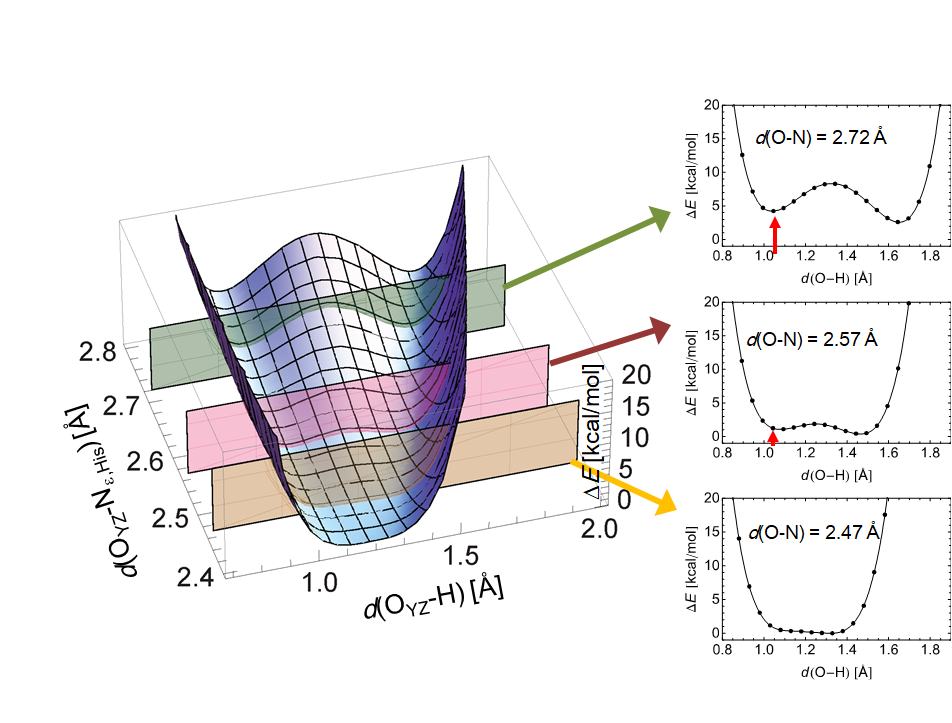
図 TyrZとD1-His190間の低障壁水素結合のドナー・アクセプター部位を遠ざけた際の水素結合ポテンシャルエナジー曲線の変化
一方、通常の水素結合の場合を以下に示します。この水素結合はphotoactive yellow protein (PYP) の基底状態におけるGlu46とp-coumaric acid間の水素結合です。低障壁水素結合とは真逆で、距離を近づけて行くにはエネルギーを要します(図、赤矢印)。また、距離を近づけていったところで、左右対称の形状にはなりません。つまり、永遠にH+が水素結合ドナーであるGlu46側に存在したままであり、p-coumaric acid側への移動はuphillです。ここから言えることは、どんなに頑張っても周辺環境が変化しない限り、一般的な水素結合は一般的な水素結合のまま。蛙の子は蛙です。また、この結果から距離だけでは低障壁水素結合であることの証明にはならないことも理解できるかと思います。
(誤解している人を見かけますが、単に「距離が近くなればプロトン移動が起こる」というのではないことがよくわかりますよね。「自発的に距離が近づくことが必要」で、そう自発的になるためには結局「pKaが一致するような周辺環境等の変化が必要」、ということです。)
PYPしか見ていなければ、おそらくこういったサイエンスはあぶり出せず、理解できないと思います。他のものと比較することで、差を感じることができる、特徴や長所・短所が浮き彫りになる。こういったことからも、自分のお気に入りの(研究)ターゲットがあればこそ、他も知りましょう。彼を知り己を知れば百戦殆うからず。孫子は現代のこういったところでも当てはまります。
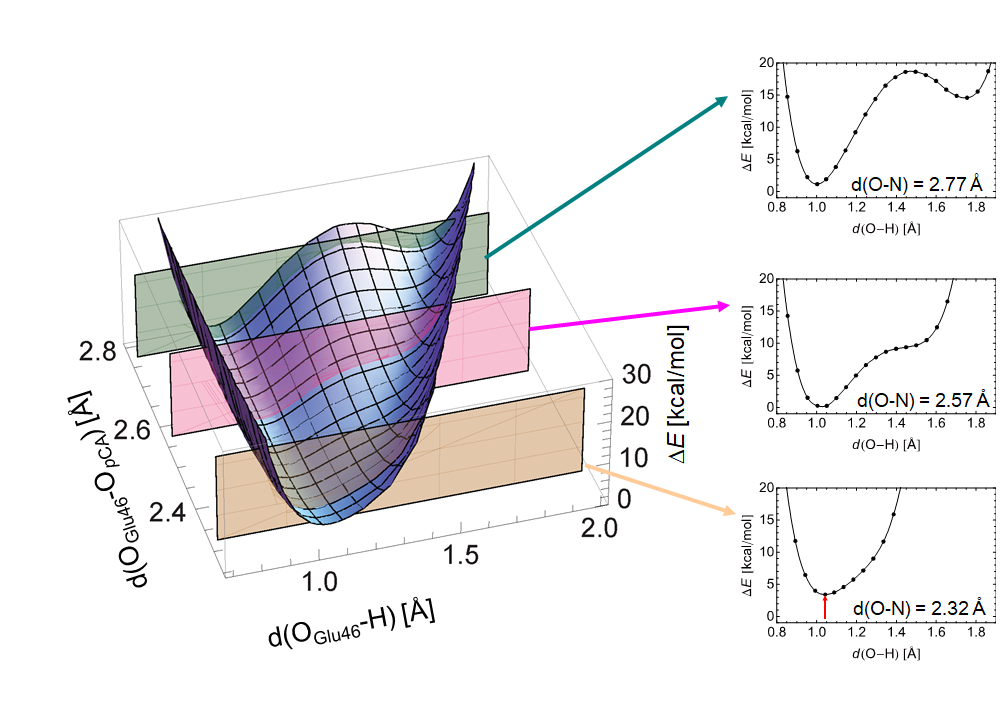
図 Glu46とp-coumaric acid間の一般的な水素結合のドナー・アクセプター部位を近づけた際の水素結合ポテンシャルエナジー曲線の変化
以上に関しては石北研究室の以下の論文ではじめて立証されました。また、とてもわかりやすく説明されていますので、引用してご利用ください。
【低障壁水素結合で距離を縮めた場合】
Keisuke Saito, Jian-Ren Shen, Toyokazu Ishida, and Hiroshi Ishikita*
Biochemistry 50 (2011) 9836-9844
“Short hydrogen-bond between redox-active tyrosine YZ and D1-His190 in the photosystem II crystal structure”
Journal Pubmed
【一般的な水素結合で距離を縮めた場合】
Keisuke Saito and Hiroshi Ishikita*
Proc. Natl. Acad. Sci. U. S. A. 109 (2012) 167-172
“Energetics of short hydrogen bonds in photoactive yellow protein”
Journal Pubmed


