色素の吸収波長変化の原因は?
光合成蛋白質には多数の色素が埋め込まれています.例えば,光合成反応に最も重要な色素であるクロロフィルaは,有機溶媒中では660 nm付近に吸収ピークを持ちますが,蛋白質の中に入ると660-700 nmに変化します.例えば,光化学系II (Photosystem II; PSII) の反応中心では,6つあるクロロフィルaの中でChlD1が最も長波長の光を吸収するいわれています.このように,同じ分子種であるクロロフィルaの吸収波長が蛋白質内でいろいろに変化する理由のひとつは「色素と蛋白質との相互作用による」とよく説明されます.具体的にはどのような相互作用なのでしょうか?
クロロフィルの周りにある蛋白質を構成するアミノ酸は,その種類により固有の電荷と分極を持っています.実はこの電荷や分極と色素との静電的相互作用が,色素の吸収波長を変化させている原因のひとつです.
周りの電荷の位置によってクロロフィルの色が変わる
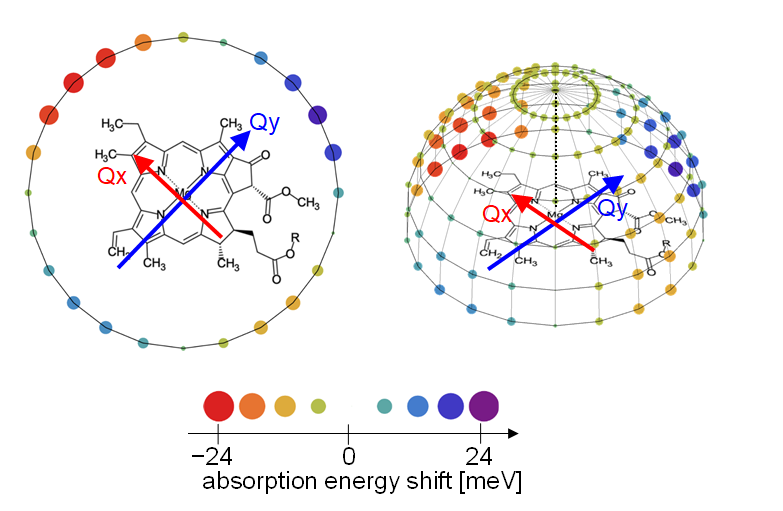
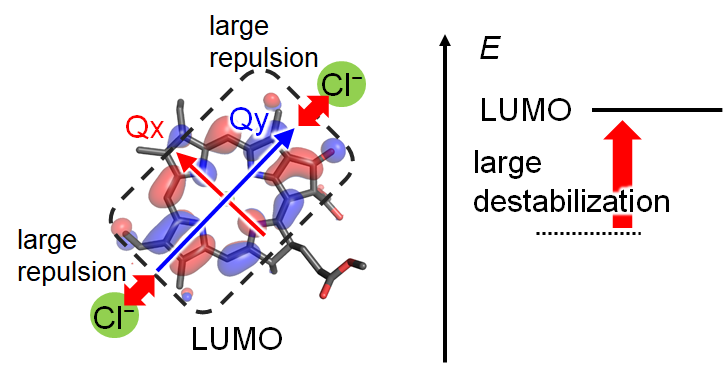
私たちは,蛋白質の電荷や分極がクロロフィルaの吸収波長にどのような影響を与えるのか,量子化学計算で調べてみました.その結果,クロロフィルの周りに存在する固有の電荷の位置によって,吸収波長の変化のしかたが異なることが明らかになりました (図1).また,変化の仕方はクロロフィルaの分子軌道のかたちによって説明できることを明らかにしました (図2).
吸収波長変化を簡単に予測する方法
これまで,蛋白質の中に入ると実際に吸収波長がどのように変化するかを調べるためには,計算コストの大きい量子化学計算が必要だと考えられてきました.しかし,上の結果を応用することで,クロロフィルの周りの蛋白質の静電的環境 (=立体構造) を調べるだけで,その吸収波長の変化を予測することができます.
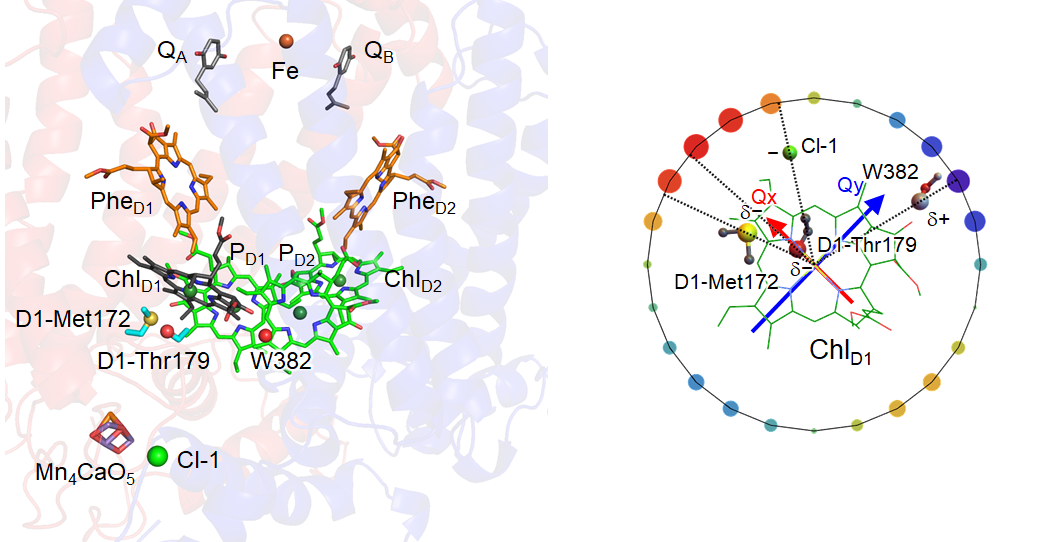
例えば,PSIIのChlD1の周りには,負電荷を持つ塩素イオン (Cl-1),負に分極した硫黄・酸素原子を持つメチオニン(D1-Met172)・トレオニン (D1-Thr179), そして正に分極した水素原子を持つ水分子 (W382) が存在しています.ChlD1が長波長の光を吸収するのはこれらが原因でした (図3).
以上の結果は、世界で初めて石北研究室が明らかにした事実であり、以下の論文に記載されています。引用してご活用ください。
Keisuke Saito*, Koji Mitsuhashi, and Hiroshi Ishikita*
J. Photochem. Photobiol. A 402 (2020) 112799. doi: 10.1016/j.jphotochem.2020.112799
“Dependence of the chlorophyll wavelength on the orientation of a charged group: why does the accessory chlorophyll have a low site energy in photosystem II?”
Journal


