蛋白質中のプロトン移動経路・水分子鎖のpKaを求める
photosystem IIでは水分解・酸素発生触媒サイトMn4CaO5錯体より水分子が水素結合で連なって一本の水素結合ネットワークを形成しています。これがO4-water chainです。
pKaはプロトン移動のdriving forceを与えるものですが、O4-water chain内の各水分子のpKaなんて求めることができるのでしょうか?ここで諦めずに私たちがとったのは次の作戦です。
1H NMRケミカルシフトに基づいたpKa計算手法開発とその応用
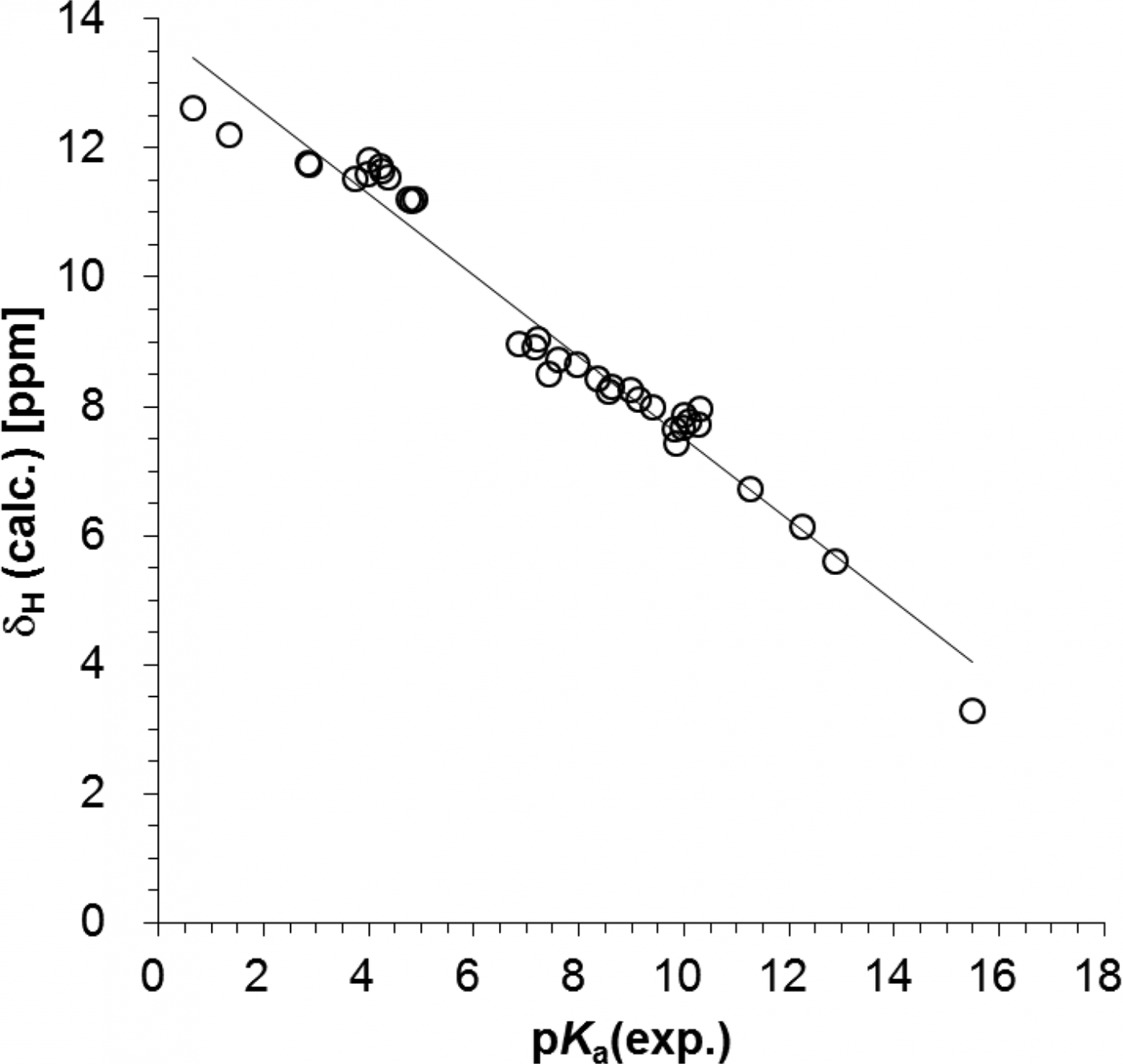
水素結合において、1H-NMRのchemical shift(δH)はプロトンがどれほどドナー側からアクセプター側へ引き寄せられているかを示す指標でもあります。この値が大きいほど、(普段はドナー側にいるのが楽なはずの)プロトンはアクセプター側に引っ張られています。(これを聞くだけでも、勘のいい人なら、水素結合ポテンシャルとの対応を頭に思い浮かべると思います。)ここから私たちは次のように考えました:「もしかしてこの性質を利用して、chemical shiftを計算することによりpKaを求められるのではないか?」。灯台もと暗しで、案外こんな基本的な研究もあまりやられていないようです。そこで本当にpKaとchemical shiftに関係があるか、様々な水素結合ペアのpKa差とchemical shiftをプロットしてみました。結果として、私たちは、このδHの値が水素結合を形成する2分子のpKaと非常によく相関することをつきとめました。
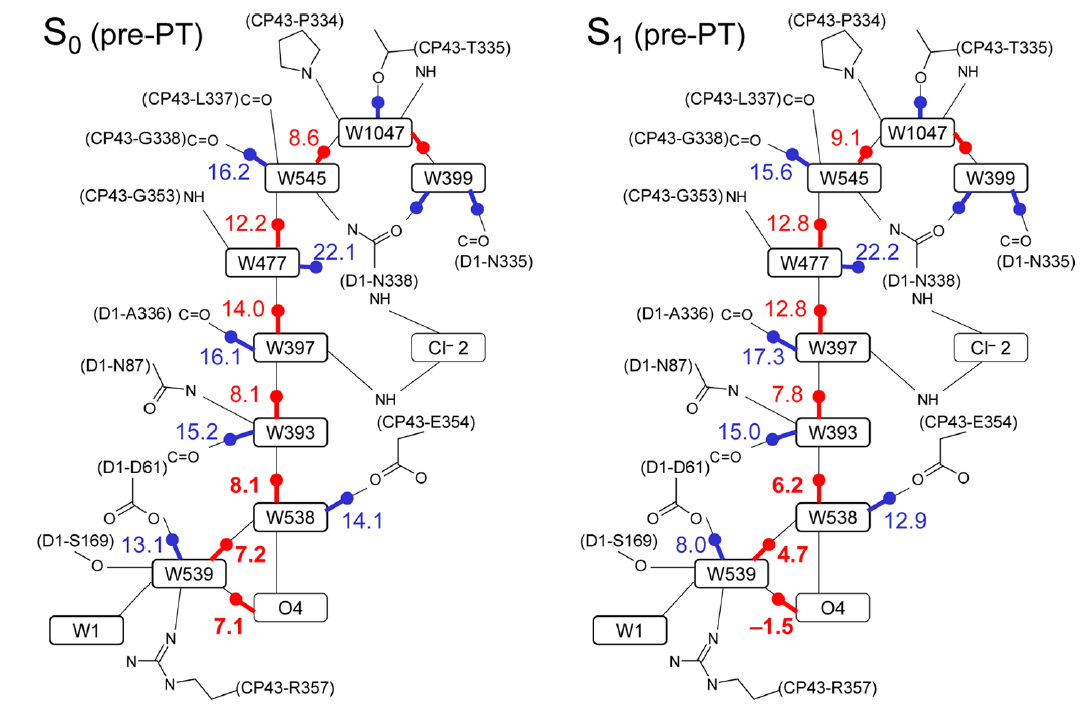
同様な手法で、蛋白質中におけるO4-water chainの水分子間のpKa差を求め、最終的にMn4CaO5錯体から水分子鎖を下っていくときにどのようにpKAが変化するかを明らかにしました。
これらの手法やpKa値は石北研究室で決定したものであり、以下の論文に記載されています。引用してご活用ください。
Tomohiro Takaoka, Naoki Sakashita, Keisuke Saito, and Hiroshi Ishikita*
J. Phys. Chem. Lett. 7 (2016) 1925-1932
“pKa of a proton conducting water chain in photosystem II”
Journal Pubmed


