photosystem IIの水分解・酸素発生触媒部位はMn4CaO5錯体と記すことが多いが、X線自由電子レーザー(X-ray free electron laser:XFEL)によって解析されたS3状態(光照射により触媒部位が2回酸化された状態)の構造には新たな第6の酸素O6がおかれており、Mn4CaO6構造と発表されています。
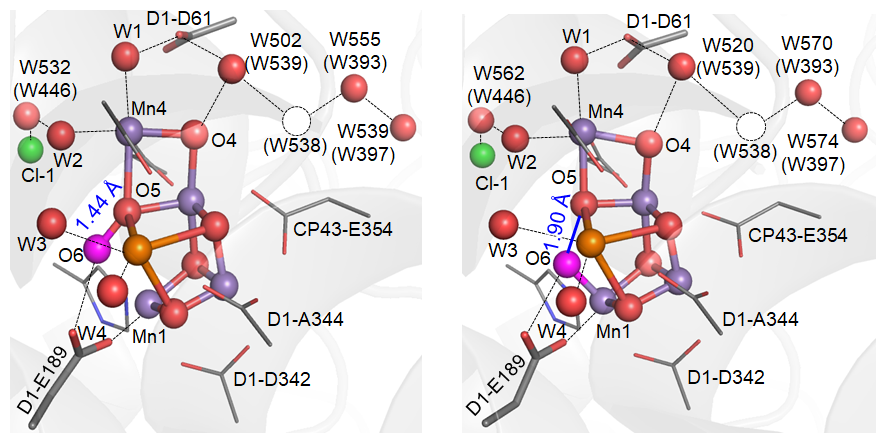
この新たにおかれたO6は近くのO5とO5…O6 = 1.9 Åというちょっと「微妙な」距離にあります。「微妙」と書いたわけがおわかりでしょうか?
- O=O:1.2 Å
- O−O:1.4 Å
- O−OH:1.5 Å
(蛋白質外の、理想的な分子種では)O原子間の距離は、共有結合を持つのであればこのようにずっと短くなります。共有結合でないのであえば、水素結合はどうでしょうか? Oを含む理想的な水素結合、すなわちH2O分子間の水素結合は2.8 Åで明らかに長すぎます。最も短いと言われている低障壁水素結合ではどうでしょうか?水分子の絡む短い低障壁水素結合は[H2O…H…OH2]+で見られますが、この場合でもせいぜい2.3 Åが限度です。
石北研究室で解析したところ、O6がO•–であるときのみ、O5…O6= 1.9 Åが再現できました。ちなみに、O6がOH–の際はO5…O6= 2.3 Åとなってしまいます。
なお、O6がOH–という議論は既にあり「近くにあるD1-Glu189がプロトン アクセプターとなりH2O → OH–が生じる」と提案されてはいますが、このプロトン移動はかなりuphillでした。その理由はD1-Glu189はMnの配位子ですので、配位部位OがH+を引き抜くという議論は、化学の基礎に立ち返れば無理がある話です。なお、少し離れたMn4の配位水W1は、この状態においてすでにD1-Asp61と低障壁水素結合をしています。
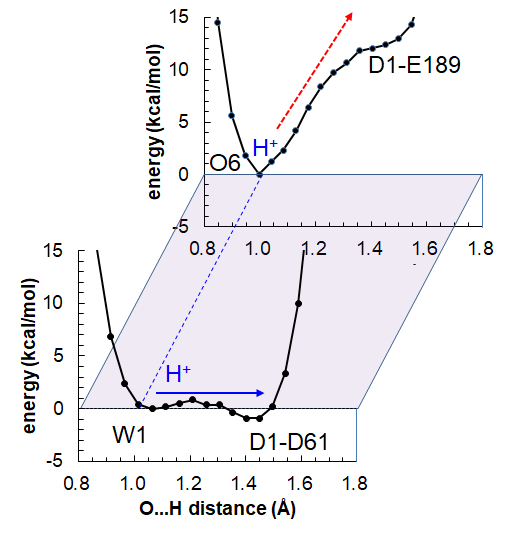
「O6がO•–」というのはどういうことなのでしょうか? 結晶構造が正しいとするなら少なくともそうでなくてはいけませんが、これが何を意味するのかは不明です。
結晶構造解析の研究では結合距離でO6の化学種を議論するしかないと思いますが、その議論を進めるのであれば「O6がO•–」でなくてはならないことが、石北研究室の研究で初めて明らかになりました。以下の論文に記載されています。引用してご活用ください。
Manoj Mandal, Keisuke Saito, and Hiroshi Ishikita*
J. Phys. Chem. Lett. 11 (2020) 10262-10268. doi: 10.1021/acs.jpclett.0c02868
“The nature of the short oxygen-oxygen distance in the Mn4CaO6 complex of the photosystem II crystals”
Journal Pubmed


